Dec 31, 2019
順藥(6535)新藥報捷 邁向臨床
順藥新藥報捷 邁向臨床
2019-12-31 23:49經濟日報 記者陳書璿/台北報導順天醫藥生技(6535)宣布,旗下治療尿毒性搔癢新藥LT5001,已經獲得台灣衛生福利部食品管理署(TFDA)審核通過,得在台灣進行一期併二期(Phase Ib/II)人體臨床試驗,順藥預計以一年時間完成Phase Ib臨床試驗,惟完成時間仍依實際執行情形而定。
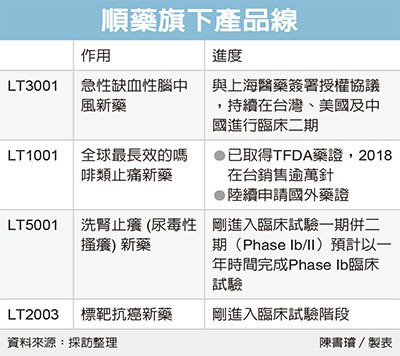
經濟日報提供
順藥指出,罹患慢性腎臟病患人數眾多,約有四成的洗腎病友飽受中度至重度不等的尿毒搔癢所苦,LT5001日後若成功上市,將可造福廣大病友。
全球洗腎病患眾多,以全球最大醫藥市場美國為例,根據美國腎臟協會統計,每七位美國人就有一位罹患慢性腎臟病,全美約有370萬慢性腎臟病患(Chronic kidney disease, CKD)。在2016年,美國有50萬人洗腎。而尿毒性瘙癢是慢性腎臟病與末期腎臟病患者 (end-stage renal disease, ESRD) 常見的併發症。根據一項名為DOPPS的跨國且持續追蹤的研究計畫(Dialysis Outcomes and Practice Patterns Study,中文:透析結果與實施類型研究),約有四成左右的洗腎病友,受中度至重度的尿毒搔癢所苦。
LT5001為順藥開發的外用劑型新藥,塗抹在患處皮膚上,可阻斷搔癢的周邊神經訊息傳遞,達到解除或大幅緩解搔癢的效果,與現行療法相較,具有安全、有效,且使用方便的優勢。根據動物試驗,LT5001至少有4小時的止癢效果,同時也證實LT5001具有約10%的經皮吸收率。
https://money.udn.com/money/story/10161/4260622

